Guten Laborpraxis (GLP): Ein Leitfaden
Erfahren Sie, was unter Guter Laborpraxis zu verstehen ist (Definition) – sowie, was deren Grundsätze sind.

Erfahren Sie, was unter Guter Laborpraxis zu verstehen ist (Definition) – sowie, was deren Grundsätze sind.

Veröffentlicht 28 Apr 2026
Artikel von
7 lesezeit
Die Gute Laborpraxis ist ein Qualitätssicherungssystem, das den organisatorischen Ablauf und die Bedingungen beschreibt, unter denen nicht-klinische Labortätigkeiten geplant, durchgeführt, überwacht, aufgezeichnet, berichtet und archiviert werden. Die GLP gewährleistet die Qualität und Integrität der gewonnen Daten, damit diese in weiterer Folge den zuständigen Behörden zur Erteilung von Forschungsgenehmigungen vorgelegt werden können.
Der Unterschied zwischen GMP und GLP liegt hauptsächlich im Anwendungsbereich. Die Gute Herstellungspraxis (GMP) gilt für den gesamten Prozess der Arzneimittelherstellung, während die Gute Laborpraxis (GLP) nur für die Phase der Sicherheitsprüfung zur Anwendung kommt. Sowohl GMP als auch GLP werden in den Vereinigten Staaten von der Food and Drug Administration (FDA) durchgesetzt.
Nachfolgend finden Sie eine Tabelle basierend auf den Vorschriften des Bundesinstituts für Risikobewertung, welche Forschungseinrichtungen bei der Entscheidung helfen soll, ob eine bestimmte Studie oder ein Experiment der Guten Laborpraxis entsprechen muss:
GLP-Konformität erforderlich | GLP-Konformität nicht erforderlich |
Studien zu Tierarzneimitteln: Studien zur Überdosierung bei der Zieltierart, Studien zur Unbedenklichkeit bei der Zieltierart, Studien zur Akkumulation und zum Abbau von Rückständen im Gewebe sowie Studien zur Euterreizung. Falls Sicherheitsstudien zur Bestimmung der potenziellen Missbrauchsmerkmale eines Prüfgegenstandes bei der FDA als Teil eines Antrags auf eine Forschungs- oder Vermarktungsgenehmigung eingereicht werden müssen. Chemische Verfahren zur Charakterisierung des Prüfgegenstandes, zur Bestimmung von dessen Stabilität und Homogenität, sowie der Konzentration von Gemischen. | Validierungsversuche zur Bestätigung der Analysemethoden, die zur Bestimmung der Konzentration des Prüfgegenstandes in tierischen Geweben und Darreichungsformen verwendet werden. Sicherheitsstudien für Kosmetikprodukte. Organoleptische Bewertung von verarbeiteten Lebensmitteln. Arbeiten zur Entwicklung chemischer Analysemethoden oder zur Festlegung der Spezifikationen eines Prüfgegenstands. Chemische Verfahren zur Analyse von Proben (z. B. klinische Chemie, Urinuntersuchungen). |
In frühen Entwicklungsphasen wie der Erforschung, dem Screening, der Grundlagenforschung und der Konzeptbewertung ist die GLP ebenfalls nicht erforderlich. Nach Angaben der Weltgesundheitsorganisation ist ihre Erfüllung in der Regel auf Stufe 2 des Arzneimittelentwicklungsprozesses beschränkt.
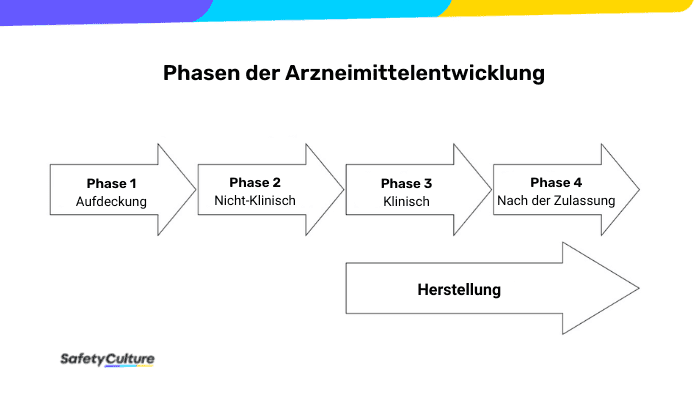
Prüfstelle oder Prüfeinrichtung: Das Forschungslabor, welches die nicht-klinische Studie durchführt. Prüfgegenstand oder Prüfobjekt: Das zu untersuchende Produkt; der Gegenstand der Prüfung. Prüfsystem: Dazu gehören
jedes Tier, jede Pflanze und jeder Mikroorganismus, bei denen der Prüf- oder Kontrollgegenstand angewendet wird.
jedes in der Studie verwendete biologische, chemische oder physikalische System.
Kontrollgegenstand oder Referenzobjekt: Ein Produkt, das
nicht der Prüfgegenstand, das Futter oder das Wasser ist.
auf das Testsystem angewendet wird.
als Grundlage für den Vergleich mit dem Prüfgegenstand dient.
Nachstehend finden Sie die Richtlinien der Guten Laborpraxis für die verschiedenen Elemente einer Studie:
Vor Beginn der Prüfung muss der Vorstand der Prüfeinrichtung einen Prüfleiter benennen, der für die Durchführung der Prüfung und die Einhaltung der GLP verantwortlich ist. Die Prüfeinrichtung muss außerdem über eine Abteilung für die Qualitätssicherung verfügen, die von der Organisation und deren Leitung unabhängig ist.
Die Prüfeinrichtung muss eine Trennung der verschiedenen Tätigkeiten vorsehen, um Wechselwirkungen und andere Störungen zu vermeiden, welche die Prüfung beeinträchtigen könnten. Es muss separate Bereiche geben für:
Die Annahme und Lagerung der Prüfgegenstände.
Das Mischen der Testartikel mit der Trägersubstanz.
Die Lagerung der daraus entstehenden Gemische.
Das Gehäuse der Testsysteme.
Alle im Rahmen der Prüfung verwendeten Geräte müssen regelmäßig kalibriert und gewartet werden. Die Aufzeichnungen über die Kalibrierung und Wartung sind aufzubewahren und den Bedienern der Geräte zur Verfügung zu stellen.
Das Personal, das die Studie durchführt, muss über jeden Prüf- und Kontrollgegenstand Folgendes wissen:
Identität, Reinheit, Zusammensetzung und Stabilität.
Empfangsdatum, Verfallsdatum und Lagerungshinweise.
Erhaltene sowie bereits verwendete Menge.
Der GLP-Prüfplan (Prüfprotokoll) ist das übergeordnete Leitdokument für die Durchführung der Prüfung. Es beschreibt, wie die Studie durchgeführt werden soll – und enthält ebenso den allgemeinen Zeitplan für sie, inklusive der Auflistung der verschiedenen Phasen. Er umfasst des Weiteren alle in der Studie verwendeten Methoden und Materialien.
Das Protokoll muss vor Beginn der Studie genehmigt, geprüft und diskutiert werden. Dieser Prozess beginnt damit, dass der Prüfleiter den Prüfplan erstellt und seinen Inhalt mit dem wissenschaftlichen Personal bespricht. Nach der Diskussion muss es vom Leiter mit seiner datierten Unterschrift genehmigt werden.
Sobald er genehmigt wurde, muss er noch von der Abteilung für die Qualitätssicherung überprüft werden, welche die Einhaltung der Guten Laborpraxis beurteilt. Zu diesem Zeitpunkt sollten die Mitarbeiter über die ihnen zugewiesenen Aufgaben unterrichtet werden und ihre eigenen Exemplare des Protokolls erhalten.
Jeder der einzelnen Bereiche der Prüfeinrichtung sollte über Standardarbeitsanweisungen (SOPs) verfügen, insbesondere für Routineverfahren. Die SOPs müssen vom Leiter der Prüfeinrichtung genehmigt werden, und alle Abweichungen von diesen vom Prüfleiter.
Für den Abschlussbericht ist letztlich der Studienleiter verantwortlich, der den Bericht ausarbeitet und genehmigt. Die wichtigsten Merkmale des Abschlussberichts sind:
Einen vollständige und genauen Übersicht über die Durchführung der Studie zu geben.
Jede Abweichung von der vorgesehenen Vorgehensweise (z. B. SOP oder Protokoll) aufzuführen.
Die wissenschaftliche Interpretation und kritische Diskussion der Ergebnisse.
Unterschriebene GLP-Konformitätserklärung des Prüfleiters.
Während des gesamten Studienverlaufs ist der Studienleiter dafür verantwortlich, dass alle relevanten Daten erfasst und in sicher aufbewahrten Unterlagen festgehalten werden. Diese Aufzeichnungen – wie das Protokoll, der Abschlussbericht und die Standardarbeitsanweisungen – werden nach Abschluss der Studie archiviert.
Nur vom Leiter der Prüfeinrichtung autorisiertes Personal kann auf archivierte Aufzeichnungen zugreifen. Darüber hinaus muss jeder Zugriff, jede Entnahme oder Rückgabe von Unterlagen in das Archiv protokolliert werden. Es wird auch empfohlen, die Archivalien zu indexieren, um das Auffinden zu erleichtern.
Die erforderliche Aufbewahrungsfrist für Prüfpläne, Versuchsprotokolle, Auswertungsergebnisse und alle anderen Dokumente einer Studie sind 20 Jahre unter Verschluss.
Nachstehend finden Sie allgemeine Beispiele für die Gute Laborpraxis:
Tragen Sie stets eine persönliche Schutzausrüstung (PSA).
Kommunizieren Sie stets mit den anderen Mitgliedern des Forschungslabors.
Regelmäßige Teilnahme an Auffrischungsschulungen und Sicherheitsübungen.
Seien Sie sich jederzeit bewusst, was Sie tun – und warum.
Achten Sie auf ungewohnte Umgebungseindrücke, wie Gerüche und Geräusche.
Verwenden Sie die richtige Laborausrüstung für die jeweilige Aufgabe.
Regelmäßige Reinigung, Kalibrierung und Wartung aller Gerätschaften.
Die GLP-Verordnungen in den USA, GROSSBRITANNIEN und der EU besitzen ähnliche Anforderungen, da diese alle Mitglieder der Organisation für wirtschaftliche Zusammenarbeit und Entwicklung (OECD) sind. Diese internationale Organisation stellte die GLP-Grundsätze auf, die heute in weiten Teilen der Welt angewandt werden.
Sorgfältige Organisation und Auswahl des Personals der Testeinrichtung.
Qualitätssicherungsprogramm.
Moderne Ausstattung und Einrichtungen.
Geeignete Testsysteme: Gerätschaften, Materialien und Reagenzien.
Klare Festlegung von Test- und Referenzobjekten.
Definierte Standardarbeitsanweisungen.
Sorgfältige Überwachung der Durchführung der Studie.
Umfangreiche Datenerfassung für die spätere Berichterstattung.
Sichere Lagerung von Unterlagen und Materialien.
SafetyCulture (vormals iAuditor) ist eine anerkannte Software für das moderne Qualitätsmanagement, welche Leiter von Prüfeinrichtungen, Studienleiter sowie die Abteilung für Qualitätssicherung und Qualitätskontrolle für die Einhaltung der GLP-Vorschriften nutzen können. SafetyCulture (iAuditor) kann bei jedem Schritt des Programms für Gute Laborpraxis eingesetzt werden, von der Erstellung des Prüfplans und des Prüfprotokolls bis zur Einreichung des Abschlussberichts .
Mit SafetyCulture (iAuditor) können Sie schnell und einfach:
Anpassbarer Vorlagen-Editor: Erstellen Sie jede Art von Checkliste oder Formular mit unseren einfach zu verwendenden Vorlagen. Erfassen Sie Ihre Daten danach bequem über unsere mobile Checklisten-App.
Einfache und doch umfassende Inspektionen: Führen Sie studienbasierte, anlagenbasierte und prozessbasierte Inspektionen mit jeglichem mobilfähigen Endgerät durch. Nehmen Sie Fotos zur Veranschaulichung auf und versehen Sie diese mit detaillierten Notizen. Weisen Sie Korrekturmaßnahmen an das zuständige Laborpersonal zu.
Elegantes, automatisiertes Reporting: Nachdem Abschluss einer Inspektion erhalten Sie automatisch einen Bericht im PDF- und Webformat. Senden Sie diesen danach mit einem Klick per E-Mail an Vorgesetzte oder speichern Sie ihn zur späteren Verwendung.
SafetyCulture (iAuditor) ist als webbasierte Software und als mobile App erhältlich. Der Download ist kostenlos – und es steht außerdem ein kostenloser Plan mit allen oben genannten Funktionen für kleine Teams zur Verfügung. Starten Sie noch heute kostenlos mit SafetyCulture (iAuditor) durch!
Studienleiter können diese Vorlage verwenden, um die Anforderungen an den Prüfplan oder das Prüfprotokoll gemäß den Vorschriften der Guten Laborpraxis (GLP) zu erfüllen. Auf der Grundlage sowohl der diesbezüglichen FDA-Verordnung als auch der OECD-Grundsätze erstellt, kannsie für folgende Aufgaben verwendet werden:
Identifizieren Sie den Prüfrahmen, den Referenzrahmen und das Prüfsystem.
Fügen Sie die Begründung für die Auswahl des Prüfsystems hinzu.
Bestimmen Sie die Dosisstufen, den Verabreichungsweg und die Dauer.
Beschreiben Sie den chronologischen Ablauf der Studie.
Listen Sie die vorzunehmenden Analysen und Messungen auf.
Studienleiter können diese Vorlage verwenden, um die Anforderungen an den Abschlussbericht gemäß den Vorschriften der Guten Laborpraxis (GLP) zu erfüllen. Auf der Grundlage sowohl der diesbezüglichen FDA-Verordnung als auch der OECD-Grundsätze erstellt, kann sie für folgende Aufgaben verwendet werden:
Änderungen und Abweichungen vom Prüfplan oder Protokoll vermerken.
Zusammenfassung, Darstellung, Bewertung und Diskussion der Ergebnisse der Prüfung.
Umstände beschreiben, welche die Qualität oder Integrität der Daten beeinträchtigt haben könnten.
Angabe der Orte, an denen der Prüfplan oder das Prüfprotokoll, Proben von Prüf- und Referenzgegenständen, Proben, Rohdaten und der Abschlussbericht aufzubewahren sind.
Fügen Sie die Erklärung zur Einhaltung der GLP und die Qualitätssicherungserklärung hinzu.
In diesem Artikel